
 |
大阪大学蛋白質研究所 蛋白質化学研究部門 |
| 詳細 |
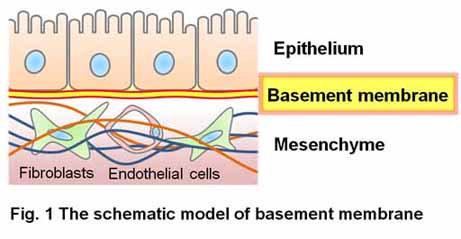
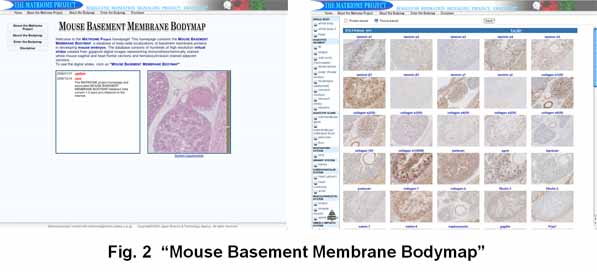
| 細胞外マトリックスは結合組織の主体である間質と、上皮と結合組織の境界に形成される基底膜に大別されますが、私たちの研究室では特に基底膜に注目しています。これは、基底膜がすべての多細胞動物に保存された細胞外マトリックスのプロトタイプであり、様々な臓器の実質を構成する上皮細胞にとって基底膜こそが直近の足場となっているからです。私たちはこれまでに同定されたほぼすべての基底膜の分子組成の全貌を明らかにしつつあります。マウス胎生16.5日胚の凍結組織切片を用いた基底膜蛋白質の網羅的な局在解析結果は、 「マウス基底膜ボディマップ (Mouse Basement Membrane Bodymap)」 (http://dbarchive. biosciencedbc.jp/archive/matrixome/bm/home.html)で公開しています (Fig. 2)。 (Manabe et al., PNAS, 2008)。 |
 |
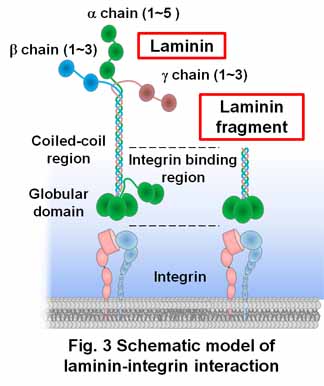
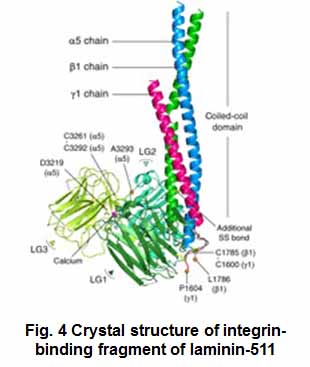
| 「ラミニン」は基底膜の主要な構成成分であり、細胞表面受容体の「インテグリン」と相互作用して、上皮細胞の機能維持や増殖・分化誘導の制御に必要なシグナルを伝達することが知られています (Fig. 3)。ラミニン-インテグリン相互作用の生理機能を明らかにするため、我々は分子レベル(結晶構造;Fig. 4, 生化学)から個体レベル(ノックアウト/ノックインマウスモデル)までの様々なアプローチに取り組んでいます。 (Nishiuchi et al., Matrix Biol., 2006; Ido et al., JBC, 2007; Taniguchi et al., JBC, 2009; Takizawa et al., Sci. Advances, 2017) |
||
 |
 |
|
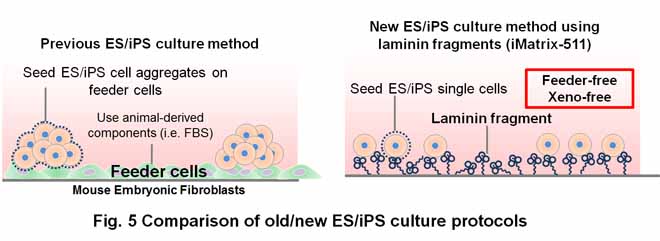
| ヒト多能性幹細胞(ES/iPS細胞)を利用した再生医療を実現するためには、これらの細胞を安全かつ安定的に培養・維持する培養技術の確立が必要です。しかし、広く使われている多能性幹細胞の標準的培養法では、マウス線維芽細胞をフィーダー細胞として使用しており、安全性に問題があることが指摘されている上に、高品質のフィーダー細胞を安定的に確保することも容易ではありません。そのため、フィーダー細胞を使わずに、ヒト多能性幹細胞を安全かつ安定的に培養する新たな培養方法の開発が求められていました。 当研究室では、京都大学の再生医科学研究所やiPS細胞研究所(CiRA)との共同研究を通じて、ラミニン511およびその活性フラグメントが、ヒトES/iPS細胞の培養基質として非常に有用であることを明らかにしています。ラミニン511はヒトES/iPS細胞に対する接着性が非常に強く、従来は困難とされていた単一細胞まで分散した状態での継代培養が可能です(Fig. 5)。特に、ラミニン511のインテグリン結合活性をほぼ100%保持した“E8フラグメント”は全長ラミニン511よりもヒトES/iPS細胞に対する接着活性が強く、これを基質に使うと、ヒトiPS細胞の樹立、拡大培養、神経細胞への分化誘導まで行うことが可能です。私たちは(株)ニッピと協力して、医療応用可能なGMP (Good Manufacturing Practice) 規格のラミニン511E8フラグメント(商品名:iMatrix-511)を製造することに成功しており、今では国内の様々な研究室で私たちのラミニン511E8フラグメントがヒトES/iPS細胞を用いた再生医療や創薬の研究に使われています。 (Miyazaki et al., Nat. Commun., 2012; Nakagawa et al., Sci. Rep., 2014; Doi et al., Stem Cell Rep., 2014) |
|
 |
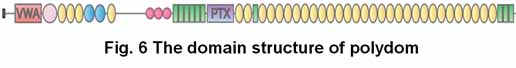
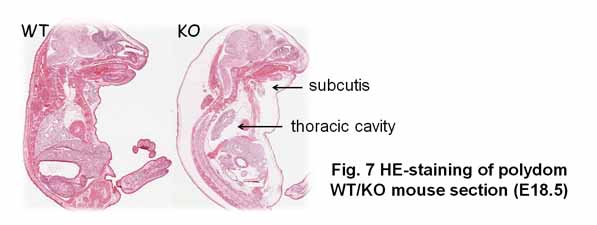
| 「Polydom」はインテグリンalpha9beta1と高親和性に結合することを我々が明らかにした、間充織に存在する細胞外マトリックス蛋白質です (Fig. 6)。(Sato-Nishiuchi et al., JBC, 2012)。 Polydomの生理的機能を明らかにするためにノックアウトマウスを作製したところ、このマウスがリンパ管形成不全のため重度の浮腫を発症して、出生直後に死亡することを見いだしました (Fig. 7)。(Morooka et al., Circulation Res., 2017) 現在、polydomノックアウトマウスのリンパ管形成不全が起こる分子基盤の解明を目指し、研究を進めています。 |
|
|
|
||
 |