チオエステル法
(Thioester method)
Merrifieldらによって開発された固相合成法は、ペプチドを迅速に化学合成するために必須の方法になっています。この方法は、アミノ酸が50残基程度のペプチドまでは効率よく合成できますが、それより長いペプチド、タンパク質になると、ペプチドの純度が極端に悪くなるため、目的物を得ることが困難になります。1991年、私たちの研究室ではこの問題を解決するため、固相法によって得たペプチド同士を必要な部位で選択的に結合し、より長いペプチド、タンパク質を得る方法(ライゲーション法といいます)、チオエステル法を開発しました(図1)。 この方法では、末端にチオエステル基を持つペプチドを鍵中間体として用います。 このペプチドのチオエステル基を銀イオンにより活性化して、別途調製した側鎖アミノ基とチオール基を保護したペプチドと縮合します。 2つのペプチドとも固相法により合成が可能なため、迅速なタンパク質合成が可能です。 この研究により、ペプチドチオエステルはタンパク質合成の鍵物質であることが広く認識されました。 現在開発されている他のライゲーション法でも、ペプチドチオエステルは鍵中間体となっています。
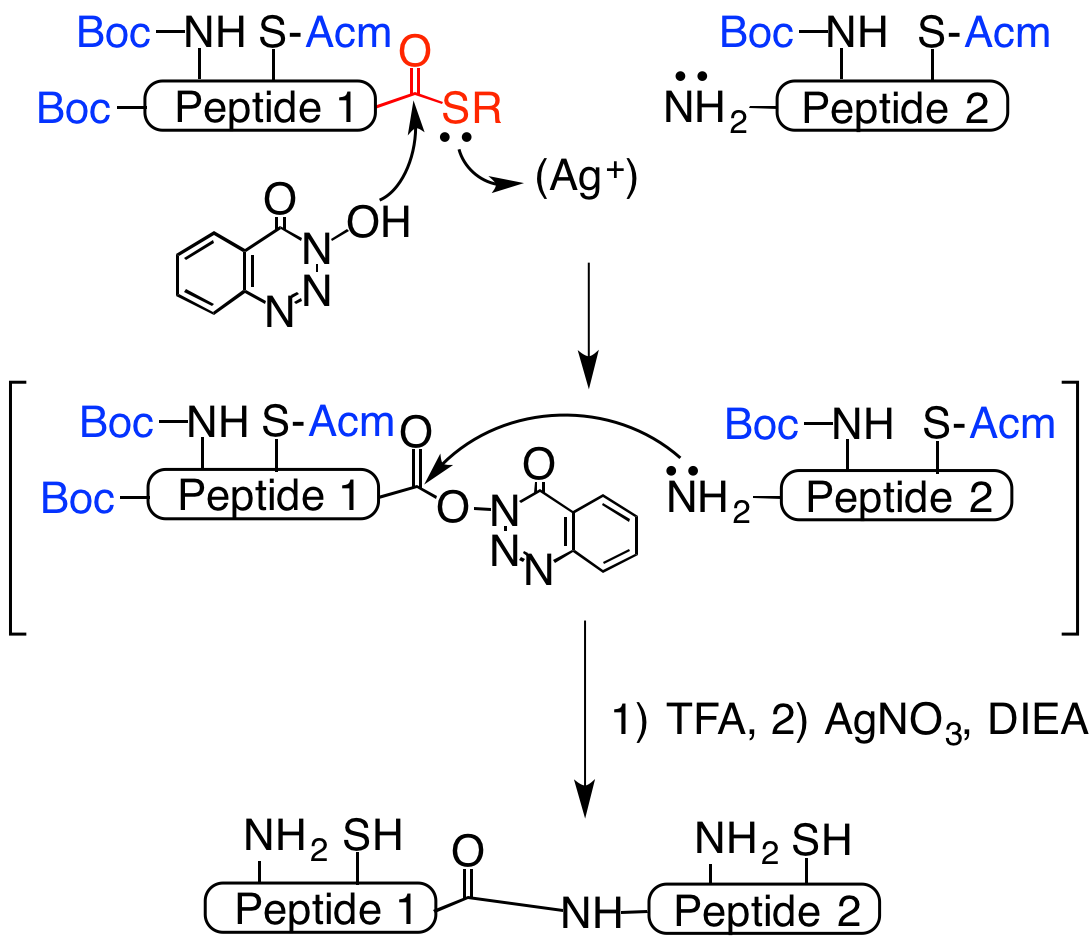
図1 H. Hojo and S. Aimoto, Bull. Chem. Soc. Jpn., 64, 111-117 (1991)
